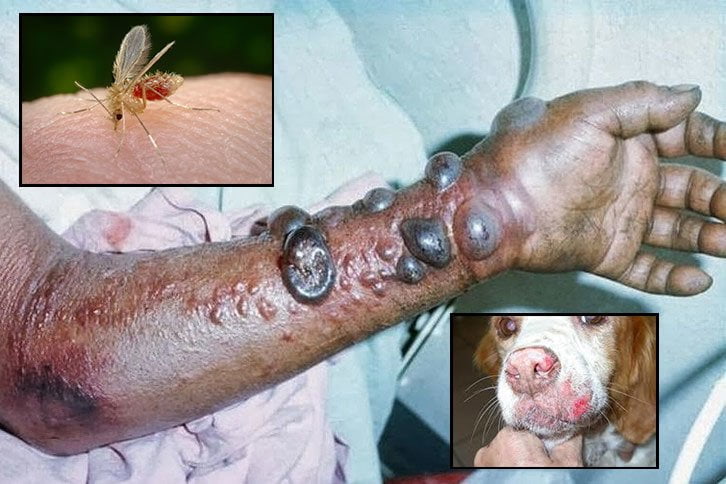
Leishmaniose Visceral ou Calazar
DESCRIÇÃO
1) HUMANA: É uma doença crônica sistêmica, caracterizada por febre de longa duração e outras manifestações, e, quando não tratada, evolui para óbito, em 1 ou 2 anos após o aparecimento da sintomatologia.
A gravidade da doença está relacionada à resposta imunológica do paciente. Desse modo, observa-se que muitos dos infectados apresentam forma inaparente ou oligossintomática da doença, e que o número de casos graves ou com o cortejo de sintomatologia manifesta é relativamente pequeno em relação ao de infectados.
Inaparente: paciente com sorologia positiva, ou teste de leishmanina (IDRM) positivo ou encontro de parasito em tecidos, sem sintomatologia clínica manisfesta.
Clássica: cursa com febre, astenia, adinamia, anorexia, perda de peso e caquexia. A hepatoesplenomegalia é acentuada, micropoliadenopatia generalizada, intensa palidez de pele e mucosas, conseqüência de severa anemia. Observa-se queda de cabelos, crescimento e brilho dos cílios e edema de membros inferiores.
Os fenômenos hemorrágicos são de grande monta: gengivorragias, epistaxes, equimoses e petéquias. As mulheres freqüentemente apresentam amenorréia.
A puberdade fica retardada nos adolescentes e o crescimento sofre grande atraso nas crianças e jovens.
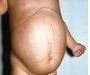
Oligossintomática: a febre é baixa ou ausente, a hepatomegalia está presente, esplenomegalia quando detectada é discreta. Observa-se adinamia. Ausência de hemorragias e caquexia.
Aguda: o início pode ser abrupto ou insidioso. Na maioria dos casos, a febre é o primeiro sintoma, podendo ser alta e contínua ou intermitente, com remissões de uma ou duas semanas. Observa-se hepatoesplenomegalia, adinamia, perda de peso e hemorragias. Ocorre anemia com Hiperglobulinemia. Geralmente não se observa leucopenia ou plaquetopenia.
Refratária: na realidade é uma forma evolutiva do Calazar clássico que não respondeu ao tratamento, ou respondeu parcialmente ao tratamento com antimoniais.É clinicamente mais grave, devido ao prolongamento da doença sem resposta terapêutica.
2) Animal:
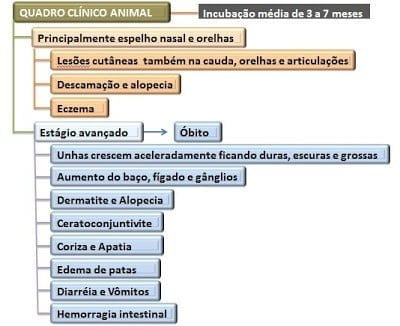
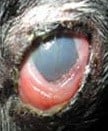

Agente: Leishmania chagasi (= infatum)
Espécies acometidas: Homens, cães, raposas, marsupiais, canídeos silvestres.
Vetor: Lutzomyia longipalpis e Lutzomyia cruzi

Período de incubação humana: 2 a 6 meses
Período patogênico: 1 a 2 anos para o óbito se não tratado. Pode recidivar após 6 meses do tratamento ter encerrado.
Período de transmissibilidade: Após 8 a 20 dias do repasto, as leishmanias evoluem no tubo digestivo destes mosquitos, que estarão aptos a infectar outros indivíduos. Não ocorre transmissão direta de pessoa a pessoa.
O homem pode transmitir a doença através dos insetos transmissores, na condição conhecida como Leishmaniose dérmica pós-calazar. A principal transmissão se faz a partir dos reservatórios animais enquanto persistir o parasitismo no sangue circulante. No reservatório infectado e não tratado é foco de contaminação enquanto viver.
Transmissão: Durante a hematofagia, introduzem no hóspede, através da saliva, um peptídeo que se considera um dos mais potentes vasodilatadores conhecidos. Estando infectado inocula os parasitas que estão na glândula salivar.

Após se infectar o parasita se multiplica no esofago e pró ventrículo e o vetor torna-se suficiente para assegurar sua inoculação em hospedeiros susceptíveis se depois o vetor voltar a alimentar-se com sangue, o crescimento dos parasitas pode ser inibido.
Mas se a segunda refeição for feita com sucos de o parasita continua se multiplicando. Quando ela ingerir sangue outra vez ele pode inocular o parasita novamente.
Após o inseto sugar o sangue infectado demora 8 dias ou mais para para se multiplicar no intestino e migrar para as probóscides (aparelho bucal). Considerando que o vetor tem um curto tempo de vida, ao redor de duas semanas ou pouco mais, ele tem que se infectar muito cedo para ter capacidade de infectar novos hospedeiros. Provavelmente ele tenha que se infectar nos primeiros repastos sanguíneos após nascerem.
Letalidade: 6,3% (2007 a 2012 – MS/SINAM). Nos pacientes não tratados a taxa de mortalidade chega a próximo de 100%.
Epidemiologia:
Sua transmissão, inicialmente silvestre ou concentrada em pequenas localidades rurais, já está ocorrendo em centros urbanos de médio porte, em área domiciliar ou peri-domiciliar. É um crescente problema de saúde pública no país e em outras áreas do continente americano, sendo uma endemia em franca expansão geográfica.
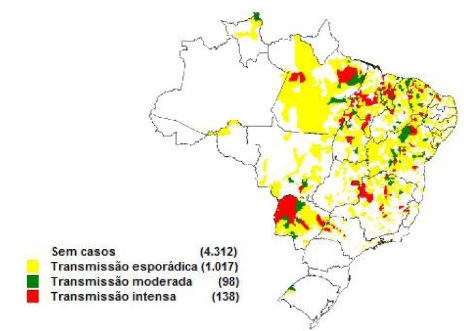
Na América Latina ela esta presente em 12 países, sendo que 90% dos casos ocorrem no Brasil.
No Brasil, a leishmaniose visceral é uma doença endêmica, no entanto tem sido registrados surtos frequentes. Inicialmente, sua ocorrência estava limitada a áreas rurais e a pequenas localidades urbanas, mas, hoje, encontra-se em franca expansão para grandes centros. A LV esta distribuída em 21 unidades da federação, atingindo as cinco regiões brasileiras. Nos últimos dez anos, a media anual de casos de LV foi de 3.379 casos e a incidência de 1,9 casos por 100.000 habitantes.
A letalidade aumentou de 3,4%, em 1994, para 5,5%, em 2008, o que representou um incremento de 61,8%. A letalidade media nos últimos 4 anos foi 6,3%.
A doença e mais frequente em menores de 10 anos (58%) e o sexo masculino é proporcionalmente o mais afetado (61%).
A razão da maior suscetibilidade em crianças é explicada pelo estado de relativa imaturidade imunológica celular, agravado pela desnutrição, tão comum nas áreas endêmicas, alem de uma maior exposição ao vetor no peridomicilio.
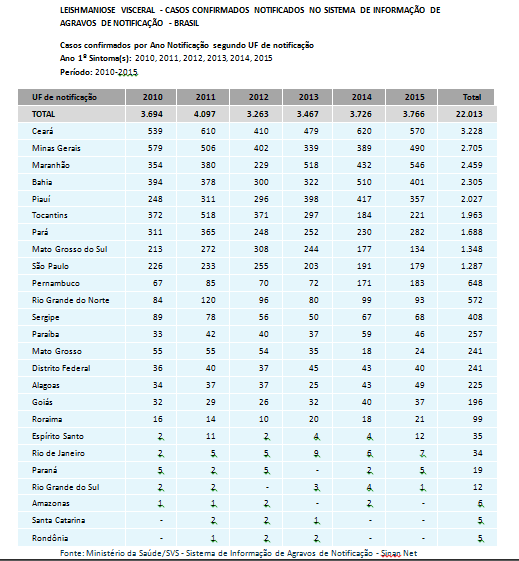
Na década de 90, aproximadamente 90% dos casos notificados de LV ocorreram na região Nordeste. Na medida em que a doença expandiu para as outras regiões, essa situação vem se modificando e, recentemente, a região Nordeste representa 48% dos casos do pais.
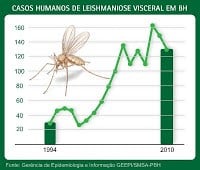
Os dados epidemiológicos dos últimos 10 anos revelam a peri-urbanização e a urbanização da leishmaniose visceral, destacando‑se os surtos ocorridos no Rio de Janeiro (RJ), Belo Horizonte (MG), Araçatuba (SP), Santarém (PA), Corumbá (MS), Teresina (PI), Natal (RN), São Luis (MA), Fortaleza (CE), Camaçari (BA) e, mais recentemente, as epidemias ocorridas nos municípios de Tres Lagoas (MS), Campo Grande (MS) e Palmas (TO) com casos autóctones em centros urbanos como Rio de Janeiro (RJ), Campo Grande (MS), Belo Horizonte (MG), Palmas (TO), Fortaleza (CE), Mossoró (RN), Salvador (BA), Araçatuba (SP), Bauru (SP), Teresina (PI) e em outras cidades de pequeno, médio e grande porte de todas as regiões do Brasil, tornando-se endêmicas nestas regiões.
No Brasil a doença se caracterizava por se apresentar em regiões tipicamente rural e principalmente nas regiões norte e nordeste. Atualmente ela vem sendo notificada e confirmada em áreas urbanas e se expandindo para as outras regiões do país.
Até 2008 a região sul nunca havia apresentado casos autócnes, todos os casos confirmados vieram de regiões endêmicas.
Em janeiro de 2009, a Secretaria Estadual da Saúde/RS notificou o primeiro caso autóctone no município de São Borja em um paciente que evoluiu para cura após tratamento.
No período de janeiro de 2009 a abril de 2010, cinco casos humanos autóctones foram detectados no estado, localizados no município de São Borja, sendo quatro adultos e uma criança. Dos cinco pacientes, quatro evoluíram para cura e um para óbito.
Até abril de 2010, foram identificados sete municípios do estado com a presença do vetor (L. longipalpis), todos localizados na fronteira com a Argentina (Barra do Quaraí, Uruguaiana, Itaqui, São Borja, Garruchos, Pirapó e Porto Xavier).
Também foram registrados 11 municípios com a presença de cães positivos sendo que cinco dessas cidades fazem fronteira com o território argentino (Barra do Quaraí, Uruguaiana, Itaqui, São Borja e Porto Xavier).
Apresenta alta letalidade em indivíduos não tratados ou com tratamentos tardios e crianças desnutridas é uma das principais doenças de importância em saúde pública da atualidade.
O aparecimento de casos humanos normalmente é precedido por casos caninos e a infecção em cães tem sido mais prevalente do que no homem.
Incidência: 20,4 casos/100.000 habitantes.
Ecologia: São insetos denominados flebotomíneos, conhecidos popularmente como mosquito palha, tatuquiras, birigui, entre outros.

A distribuição geográfica de é ampla e parece estar em expansão, se deslocando de ambientes rurais para ambientes urbanos. Essa espécie e encontrada nas cinco regiões geográficas do país, sendo que, na região Sul, o primeiro registro ocorreu em dezembro de 2008.
A L. longipalpis adapta-se facilmente ao peridomicilio e a variadas temperaturas, podendo ser encontrada no interior dos domicílios e em abrigos de animais domésticos. Ha indicio de que o período de maior transmissão da leishmaniose visceral ocorra durante e logo após a estação chuvosa, quando ha aumento da densidade populacional do inseto.
Seu habitat é o domicílio e o peridomicílio humano onde se alimenta de sangue do cão, do homem, de outros mamíferos e aves. As fêmeas têm hábitos antropofílicos, pois necessitam de sangue para a maturação dos ovócitos.
A atividade dos flebotomíneos e crepuscular e noturna. No intra e peridomicilio, a L. longipalpis e encontrada, principalmente, próxima a uma fonte de alimento. Durante o dia, esses insetos ficam em repouso, em lugares sombreados e úmidos, protegidos do vento e de predadores naturais.
Controle: Tratamento humano que dependendo da medicação pode levar até 40 dias. A Leishmaniose visceral canina é mais resistente à terapia do que a terapia humana e a cura parasitológica é raramente obtida.
Atualmente o MAPA não tem nenhum medicamento liberado para o tratamento de cães. Além disto, a Portaria Interministerial nº 1.426/2008, proíbe o tratamento de cães com produtos sem registro no MAPA, bem como a importação de medicamentos para tratamento de LVC. Deste modo, tanto o proprietário do cão quanto o médico veterinário estarão sujeitos às penalidades previstas caso desrespeitem a referida Portaria.
Além disto a Portaria Interministerial nº 1.426/2008 proíbe o uso de medicamentos humanos para tratamento canino de leishmaniose. Essa proibição deve-se ao fato de que o uso rotineiro dessas drogas no tratamento de cães, favorece o surgimento de protozoários resistentes. As drogas disponíveis para tratamento humano da leishmaniose visceral são poucas, se o parasita criar resistência a elas poderia ficar muito difícil tratar os casos humanos e isso aumentaria o número de óbitos.
Se o cão tiver sido tratado e não apresentar parasitas na biópsia da pele nem sorologia positiva ou se a titulação tiver diminuído ou os exames laboratoriais tiverem normalizado, não significa que está curado e não oferece mais risco.
Infelizmente não há comprovação de que os diferentes esquemas de tratamento utilizados, mesmo sem a recomendação da Portaria Interministerial nº 1.426/2008, sejam capazes de eliminar totalmente os parasitas. É sabido que a interrupção do tratamento muitas vezes faz com que os sintomas reapareçam e, embora a melhora do quadro clínico e laboratorial seja esperada, não é uma condição definitiva. Apenas prolonga o sofrimento, adia a decisão de eutanasiar o animal, prolongando também o risco epidemiológico de transmissão do parasita.
O isolamento de Leishmania chagasi/infantum na medula óssea, gânglio, fígado, baço ou pele é o padrão para o diagnóstico parasitológico de certeza da contaminação. Porém, os testes sorológicos também são confirmatórios quando são feitos dois exames de sangue: o teste rápido e o ELISA ou IFI. O teste rápido, também chamado de DPP, é altamente específico e fornece resultado em meia hora. Se ele for negativo é garantia de que o cão não está doente, mas se ele for positivo pode existir uma pequena chance desse resultado ser falso.
Por isso é necessário repetir o exame usando o teste de ELISA, sendo ele também positivo, confirma o diagnóstico. Portanto o diagnóstico é confirmado com testes rápidos DPP positivo e ELISA positivo, realizados em laboratório público oficial de referência (Laboratório Central do Estado – LACEN).
Todo cão com sorologia positiva, sintomático ou não, oferece risco à comunidade, pois carrega na pele o parasita que causa a leishmaniose visceral. Havendo flebótomos (mosquitos-palha) onde há cães positivos existem as condições para a transmissão da doença. Portanto, todo cão com sorologia positiva tem que ser submetido à eutanásia, o que está de acordo com a Resolução nº 1000, de 11 de maio de 2012 do Conselho Federal de Medicina Veterinária – CFMV, Capítulo 1, Artigo 3, inciso II.
Conforme a Portaria Interministerial nº 1.426/2008, é proibido o tratamento de cães com LV. Neste sentido, o não cumprimento implica em infração ao código de ética do Médico Veterinário em seu artigo 13 inciso XXIII, entre outros. As penalidades previstas variam desde advertência sigilosa até a cassação do registro profissional.
Os flebótomos ou ‘mosquitos-palha’ não são mosquitos comuns. Vivem e se criam em lugares úmidos, sombreados, protegidos do vento e com solo rico em matéria orgânica. Aproximam-se dos seres humanos e animais para se alimentar. Como são muito pequenininhos, medindo cerca de 2 a 3 mm, só podem ser contidos por telas de malha muito fina.
Medidas simples como limpeza dos terrenos e quintais, eliminação de resíduos orgânicos do solo, entrada da luz solar, redução da umidade do solo, afastamento dos abrigos dos animais domésticos das casas, podem ajudar a diminuir a quantidade destes insetos. A aplicação de inseticidas só está indicada em situações especiais, de acordo com a avaliação da Vigilância Epidemiológica e deve ser realizado por empresas especializadas.
As pessoas podem se proteger das picadas usando repelentes e evitando permanecer nas áreas externas durante o entardecer ou período noturno.
Para evitar a disseminação da doença entre cães são necessários alguns cuidados. Em primeiro lugar está o controle da população de cães errantes que deve ficar sob a responsabilidade do município, segundo as normas vigentes no Código Sanitário.
Todos estes cães devem ser testados para LVC antes de serem encaminhados para doação. Em segundo lugar estão as medidas de proteção para evitar a picada de flebótomos, como a telagem de canis individuais e coletivos, sobretudo os canis de clínicas veterinárias, abrigos de animais, hospitais veterinários e canis públicos, com tela de malha muito fina.
Todo cão suspeito de ser portador de leishmaniose visceral canina deve ser reportado à Vigilância Epidemiológica do município para proceder à investigação do caso, conforme fluxo para notificação e investigação de caso suspeito de LVC no link http://www.dive.sc.gov.br/conteudos/zoonoses/Vetores/leishmanioses/Guia_Basico_de_Orientacao_Leishmaniose_Visceral_Canina.pdf.
Segundo o fabricante da vacina liberada recentemente pelo Ministério da Agricultura Pecuária e Abastecimento a vacina deverá ser usada somente em cães assintomáticos com resultados sorológicos negativos para Leishmaniose Visceral.
A vacina não protege 100% dos cães, portanto, animais vacinados podem adquirir a infecção e se tornarem portadores infectantes para o vetor.
A vacinação não é o único instrumento de prevenção e controle desta enfermidade. Outras medidas devem ser adotadas conforme normatização do Ministério da Saúde. Os animais que apresentarem sinais clínicos de Leishmaniose Visceral e reações sorológicas positivas estarão passíveis das medidas sanitárias vigentes.
Desta forma, esta vacina torna-se a ÚNICA vacina no Brasil a cumprir a determinação da Instrução Normativa Interministerial Nº31/2007 e ter o Estudo de Fase III aprovado pelas duas instituições de vigilância e controle da Leishmaniose Visceral no Brasil.

Leishmaniose Tegumentar Americana
DESCRIÇÃO:
1) Humano: A doença pode se apresentar de três formas diferentes a cutânea, a mucosa e a mucocutânea.
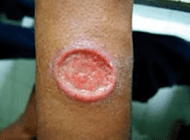
Na cutânea ou tegumentar (úlcera de Baurú, leihsmaniose tegumentar americana – LTA) as lesões de pele pode ser única ou múltipla, disseminada (lesões muito numerosas em várias áreas do corpo) e a forma difusa.
Na maioria das vezes a doença apresenta-se como uma lesão ulcerada única. Nas formas localizada e disseminada, a lesão ulcerada franca se caracteriza por úlcera com bordas elevadas, em moldura. O fundo é granuloso, com ou sem exsudação. Em geral, as úlceras são indolores.
Observam-se também outros tipos de lesão como úlcero-crostosa, impetigóide, ectimatóide, úlcero-vegetante, verrucosa, tuberosa, linquenóide e outras. Nestas formas, na fase inicial, é freqüente a linfangite e/ou adenopatia satélite, que poderia preceder a lesão de pele.
As formas localizada e disseminada costumam responder bem à terapêutica tradicional.
Na forma difusa, rara, as lesões são papulosas ou nodulares, deformantes e muito graves, distribuindo-se amplamente na superfície corporal. Evolui mal por não responder adequadamente à terapêutica.
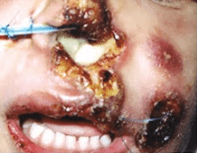
A apresentação mucosa é na maioria das vezes secundária às lesões cutâneas, surgindo geralmente meses ou anos após a resolução das lesões de pele atingindo, principalmente, as cavidades nasais, seguidas da faringe, laringe e cavidade oral precedido de queixa de epistaxes, rinorréia e crostas; da faringe com ingestão de alimento dolorosa; da laringe com rouquidão e tosse; da cavidade oral com ferida na boca.
As mucosas atingidas apresentam ulceração, perfuração do septo nasal, lesões ulcero vegetantes, ulcero crostosas em cavidades nasal, ulcero destrutivas.
Poderá ocorrer destruição parcial ou total da pirâmide nasal e outras estruturas acometidas na boca. Outras mucosas, como língua e órgãos genitais, são raramente atingidas.
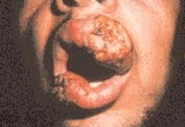
A apresentação mucocutânea da LTA em que se verifica a presença de lesões associadas na pele e na mucosa, pode ser concomitante (o acometimento mucoso à distância da lesão ativa em pele), ou contígua (o comprometimento mucoso ocorre por extensão da lesão de pele situada próxima de mucosas).
O diagnóstico precoce de lesão mucosa é essencial para que a resposta terapêutica seja mais efetiva e sejam evitadas as seqüelas deformantes e/ou funcionais.
2) Animal:

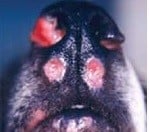
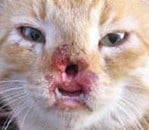
Agente: Leishmania brasiliensis – leishmaniose tegumentar americana, leishmaniose cutâneo mucosa, úlcera de Baurú.
Espécies acometidas: cães e raposas (portadores permanentes), equinos, gatos, roderores, preguiça, tamanduá, marsupiais, lobo guará, graxaim (sorro).
Vetor: Phlebotomus spp (velho mundo – Europa e demais)), Lutzomyia (Novo mundo – Américas) chamados de mosquito palha, birigui.

Período de incubação: 2 a 4 meses no homem e 8 a 20 dias no mosquito. A calazar vai de meses a anos.
Período patogênico: não tratada evolui para óbito em 1 ou 2 anos
Período de transmissibilidade: o vetor poderá se infectar enquanto persistir o parasitismo na pele ou no sangue circulante dos animais reservatórios. No homem é desconhecido.
Transmissão: picada do vetor infectado de reservatórios que apresentam feridas no corpo além de transfusional e congênita.
Letalidade: 0,1% (2006 A 2012 – MS/SINAM)
Epidemiologia: Nas ultimas décadas, as analises de estudos epidemiológicos da LTA demonstram mudanças no comportamento epidemiológico da doença.
Inicialmente considerada zoonose de animais silvestres, que acometia ocasionalmente pessoas em contato com florestas, a LTA começa a ocorrer em zonas rurais já praticamente desmatadas e em regiões periurbanas.
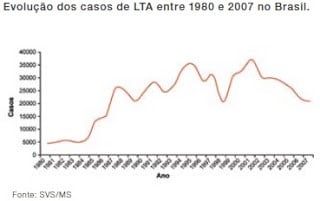
No período de 1988 a 2007, a LTA apresentou media anual de 27.736 casos autóctones registrados e coeficiente de detecção médio de 17,3 casos por 100.000 habitantes. Ao longo desse período, observou-se uma tendência no crescimento da endemia, registrando os coeficientes mais elevados nos anos de 1994 e 1995, quando atingiram níveis de 22,83 e 22,94 casos por 100.000 habitantes, respectivamente.
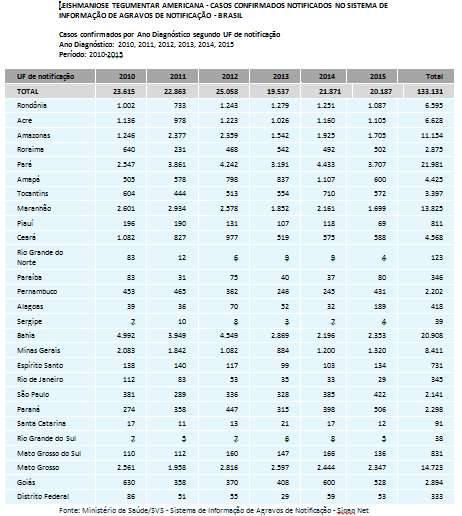
Ao analisar a evolução da LTA no Brasil, observa-se uma expansão geográfica, sendo que, no inicio da década de 80, foram registrados casos autóctones em 19 unidades federadas e, no ano de 2003, foi confirmada autoctonia em todas as unidades federadas do pais.
A região Norte vem contribuindo com o maior numero de casos (cerca de 36,0% do total de casos registrados, no período) e com os coeficientes médios mais elevados (85,4 casos por 100.000 habitantes), seguida das regiões Nordeste (43,5 casos por 100.000 habitantes) e Centro-oeste (37,5 casos por 100.000 habitantes).
A partir do indicador da densidade de casos, identificou-se, no período de 2004 a 2006, 26 circuitos de produção da doença de importância epidemiológica, os quais foram responsáveis por 56,9% do total de casos registrados em 2007, distribuídos em 663 municípios do total de 1.803 que apresentaram casos em todo o pais.
A LTA é uma zoonose amplamente distribuída no território brasileiro, ocorrendo em todas as regiões do país. Surtos epidêmicos têm ocorrido nas regiões Sudeste, Centro-Oeste, Nordeste, Norte e, mais recentemente, na região Sul.
Organização Mundial da Saúde (OMS) considera esta enfermidade como uma das seis mais importantes doenças infecciosa de distribuição mundial.
No Estado do Paraná a LTA é endêmica, desde os primeiros casos registrados na década de 40, associada a L. braziliensis. Nos estados de SC e RS há uma nítida expansão com um significativo aumento nos últimos anos.
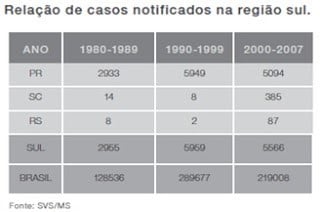
No início da década de 80, foram registrados casos autóctones em 19 unidades federadas e, no ao de 2003, foi confirmada autoctonia em todas as unidades federadas.
No estado do Paraná, 276 dos 399 municípios tem endemicidade, principalmente nas regiões norte e oeste.
Incidência: Nos últimos anos, o Ministério da Saúde registrou média anual de 35 mil novos casos de LTA no país.
Ecologia: Doença inicialmente de distribuição rural, encontra-se em franca expansão para focos urbanos no Brasil onde existem grandes áreas florestais. O vetor ataca ao por do sol e à noite. Fazem pequenos vôos e pousam é como se estivessem saltitando. Voam entre 100 e 150m.
Sua densidade aumenta com umidade (80% ou mais), calor (20° a 30°C), sem vento e muita MO em decomposição como folhas, raízes, frutas, excretas de animais e comida (sangue e seiva) para oviporem e viverem. Os adultos podem ser encontrados nas copas e solo.Diminui nos períodos secos e inverno e aumenta nos dias quentes e chuvosos
Controle: Controle de cães vadios, conhecer se a área de mata em que for visitar se tem presença da doença.
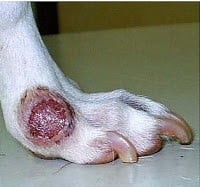
Segundo o Manual de vigilância e controle da LTA do Ministério da Saúde, 2007, a eutanásia é indicada quando os animais doentes evoluem para o agravamento das lesões cutâneas com surgimento de lesões mucosas e infecções secundárias que poderão conduzir o animal ao sofrimento
O tratamento de animais doentes não e uma medida aceita para o controle da LTA, pois poderá conduzir ao risco de selecionar parasitos resistentes as drogas utilizadas para o tratamento de casos humanos.
Atualmente existe apenas uma vacina que, após ser analisada pelo Ministério da Agricultura, Pecuária e Abastecimento (MAPA) e pelo Ministério da Saúde (MS), obteve autorização para ser fabricada e comercializada.
Esta vacina é uma vacina Recombinante contra Leishmaniose Visceral Canina composta por antígeno de Leishmania sp . produzido em Escherichia coli sob a forma de proteína recombinante capaz de induzir resposta imunológica contra Leishmania donovani, L. infantum, L. chagasi, L. amazonensis e L. mexicana .
Verifica-se que esta vacina está indicada para o controle preventivo de leishmaniose visceral e não a tegumentar. Não há informações se ela tem ação sobre a Leishmania braziliensis desta forma o veterinário deverá ser consultado para avaliar cada situação e indicar ou não o uso desta vacina.
Tratar os cães doentes ou soro positivos não ajuda a controlar a disseminação da doença, pois os cães tratados melhoram temporariamente, mas continuam com o parasita na pele mesmo estando sem sintomas, porque são os reservatórios naturais deste parasita sendo fonte de infecção para os flebótomos e oferecerá risco de transmissão de leishmaniose visceral para as pessoas.
Em 2012 um caso chamou atenção pela repercussão tomada devido à decisão legal de eutanásia de um cão infectado por leishmaniose cujos resultados devem servir para a tomada de decisões uma vez que decisões erradas podem levar a consequências graves.
Ano passado (2012 o cachorro Scooby ficou conhecido por ter sido arrastado pelo dono, de moto, até o CCZ. Lá ele foi diagnosticado com leishmaniose e a partir daí começou um apelo da comunidade pela não eutanásia chegando a ser discutido legalmente este posicionamento profissional cuja notícia se encontra abaixo.
Entretanto não foi citado que tipo de leishmaniose o cão tinha. Por esta razão vamos repetir esta notícia quando falarmos em leishmaniose visceral uma vez que esta medida de eutanásia para cães com leishmaniose é orientada para ambos casos e que pode ser encontrada no link abaixo:
A médica veterinária Maíra Kaziski Peixoto, nova presidente da ONG Abrigo dos Bichos, protocolou nesta sexta-feira (4) um ofício na Secretaria Municipal de Saúde (Sesau) pedindo informações em até 24 horas sobre o paradeiro e estado de saúde do cão Scooby. O bicho ficou conhecido após ter sido amarrado em uma moto e arrastado pelo dono até o Centro de Controle de Zoonoses (CCZ).
Logo após chegar ao centro, um exame atestou que o bicho tem leishmaniose. Na época, o órgão cogitou encaminhar o bicho para a eutanásia, conforme estabelecem normas do Ministério da Saúde.

Internautas fizeram campanha para que Scooby não fosse sacrificado. O mascote foi levado a uma clínica veterinária no dia 30 de julho de 2012, com autorização da prefeitura de Campo Grande, para que recebesse tratamento contra a doença.
No dia 19 de dezembro, o ex-prefeito de Campo Grande Nelson Trad Filho (PMDB) pediu que o cão fosse devolvido ao CCZ, onde passaria por exames comprovando a melhoria do estado de saúde e eficiência do tratamento contra a doença.
A assessoria do Abrigo dos Bichos informou que, após entregar o animal para o CCZ, a ONG não recebeu mais nenhuma informação sobre Scooby.
De acordo com diretora de Vigilância em Saúde da Secretaria Municipal de Saúde (Sesau), Márcia Dal Fabbro, a ONG protocolou o pedido por volta das 15h30. Segundo ela, a resposta será encaminhada até a segunda-feira por meio de nota técnica.
Uma decisão do Tribunal Regional Federal da 3ª Região autoriza o tratamento da leishmaniose visceral em cães em todo o país. O pedido de liberação foi feito em ação movida pela ONG Abrigo dos Bichos, sediada em Campo Grande. A sentença suspende os efeitos da portaria do Ministério da Agricultura, Pecuária e Abastecimento (Mapa) que proíbe a utilização de medicamentos de uso humano no tratamento de cães infectados pela doença. Ainda cabe recurso da decisão, que foi publicada no Diário da Justiça Federal da 3ª Região na última quarta-feira.

A decisão é da 4ª Turma do TRF 3ª Região, concedida pela maioria dos desembargadores no dia 16 de setembro de 2012, porém, só tem validade a partir da publicação do acórdão, o que foi feito apenas no dia 16 de janeiro de 2013 no site do Tribunal de Justiça em Mato Grosso do Sul cabendo lembrar que é válida para todo território Nacional,
A assessoria de imprensa do Mapa informou que não foi notificada oficialmente sobre a decisão judicial, e assim que isso ocorrer, técnicos do órgão irão discutir o assunto.
O Conselho Regional de Medicina Veterinária (CRMV-MS) informou que a decisão não muda as orientações do órgão, que é contra o tratamento da doença. “É preciso estabelecer que a portaria regulava a atuação dos órgãos de saúde pública com relação ao controle da doença. Até que haja o reconhecimento da comunidade científica sobre a cura da doença, ou o registro dessas drogas, que possibilitem a mudança de posicionamento do conselho federal, qualquer médico veterinário do estado que insistir em lançar mão do medicamento, estará transgredindo o código de ética.”, diz o presidente do órgão, Eduardo Marcondes.
Scooby foi levado a uma clínica veterinária para receber tratamento contra a doença, com autorização da prefeitura de Campo Grande.
No ano passado, a veterinária Sibele Cação, então presidente do CRMV-MS, defendeu publicamente o tratamento contra a leishmaniose em cães e, por conta disso, foi destituída do cargo. Ela disse que, após cinco meses de tratamento, o vira-lata não tinha mais os sintomas da doença.